金属の「腐食」を「錆び」と言います。
なぜ錆びるの?
様々な製品に使用されている金属材料ですが、加工された金属は非常に不安定で腐食(酸化)によって元の安定状態に戻ろうとします。これが「錆」です。錆は発生するとその金属部品は使用不可能になってしまう場合もあり使用環境や用途に応じて対策が必要となります。
●腐食のメカニズム
- 大気中の酸素によって金属表面には極薄の酸化皮膜が形成されています。
- 大気中には酸素以外にも、水分や埃、汚染物(イオン、有機酸等)が存在しています。
金属表面にそれらの物質が付着することで酸化皮膜が破壊され、腐食が進行していきます。
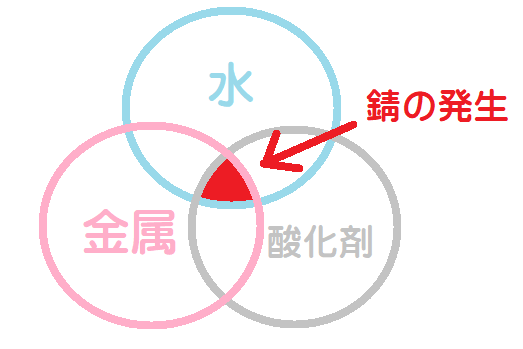
① 酸化剤(大気中に存在する酸素や水分中の H+等)
② 腐食される金属
③ 水
上記3 条件が重なった環境下で腐食は進行していきます。
●腐食の種類
- 均一腐食
- 金属表面全面の発生する腐食
酸に浸漬した場合の鉄の腐食、大気中での鉄の錆などや銀の表面変色など - 局部腐食
- 局部的な腐食で発見しにくく特定し難い。
一般的な製造部品などで問題になる錆による損傷は、殆どが局部的腐食。
材質、 表面処理、使用環境や物理的負荷により、さまざまな局部腐食が発生する。
錆びを防ぐ(防食)一つの方法が「表面処理」です。
金属製のねじはほとんどの場合で、腐食を防ぐために成型後に何らかの表面処理を施します。表面処理は、素材の硬さ、耐摩擦性、耐食性、潤滑性などを加え、美観についても向上させる働きがあります。
この表面処理の代表的なものが【めっき処理】です。
めっきとは材料の表面に他の金属の薄い膜をかぶせる処理のことを言います。
Point 金属のイオン化傾向
めっきの素地金属に対する耐食性を知るためには、
金属のイオン化傾向を知ることが必要です!
金属には種類によって溶解しやすさ(錆びやすさ)に差があり、
これを順位付けしたものをイオン化傾向といいます。
イオン化傾向の大きいもの=イオンになりやすい(溶解しやすい・錆びやすい)金属を「卑な金属」
イオン化傾向の小さいもの=イオンになりにくい(溶解しにくい・錆びにくい)金属を「貴金属」
| イオン化傾向 (大) 錆びやすい |
イオン化傾向 (小) 錆びにくい | |||||||
|---|---|---|---|---|---|---|---|---|
| Al アルミ |
Zn 亜鉛 |
Fe 鉄 |
Ni ニッケル |
Sn スズ |
Pb 鉛 |
Cu 銅 |
Ag 銀 |
Au 金 |
●メッキの処理方法
- 電気めっき
- 電解液中で金属材料の品物をマイナス極に通電し表面に金属を付着する方法。
密着性◎、厚さの調整が可能、外観が良好、めっきの種類が多い、大量生産が可能
例:亜鉛めっき、ニッケルメッキ、クロームめっきなど - 無電解めっき
- 品物に通電することなく、メッキ液中の金属イオンを還元剤の働きで品物の表面に析出し金属の膜を付着させる方法。均一な膜厚が得られる。樹脂などの不導体にもメッキ可能。
例:無電解ニッケルメッキ など - 溶融めっき
- 亜鉛やスズ、アルミなどの金属を溶融(加熱し液状にする)しためっき浴に品物を入れ、溶融した金属を付着させる方法。面積の大きな品物、重量物の防食めっきに適している。
例:ドブメッキ など - 陽極酸化処理
- 硫酸や硝酸などの電解溶液中で品物を陽極とし、通電して表面に酸化被膜を生成させる。
陽極酸化とめっきの違いは品物を陽極とするか陰極とするかの違いです。
着色可能なので、用途が幅広く、アルミ製品でよく利用されています。
例:アルマイト処理 など - 化成処理
- 化学反応を利用して、溶液中で品物の表面に薄い酸化膜や硫化膜を生成する。防錆したり、塗装との密着性を向上させることができる。
例:クロメート処理、パーカー処理 など 【表面処理】早見表はこちら
より詳しく知りたい方はこちら⇩
ねじの基本知識

小ねじ類 |

ボルト類 |

キャップ類 |

ナット類 |

ワッシャー類 |

緩み止め |

ピン・リング類 |

樹脂製品 |

プレコート加工 |

自衛ねじ |

止めねじ |

頭部塗装 |

建材用ねじ(ドリルねじ・タッピンねじ) |

リベット |

アンカー |

工具類 |

クリンチング |
機能ねじ |

寸切りボルト |

止め輪類 |